Επιτυχής Θεραπεία της Νόσου Χάντινγκτον για Πρώτη Φορά

Μία από τις πιο σφοδρές και καταστροφικές ασθένειες – η νόσος Χάντινγκτον – έχει θεραπευτεί με επιτυχία για πρώτη φορά, λένε οι γιατροί.
Η ασθένεια διατρέχει τις οικογένειες, αδιάκοπα σκοτώνει εγκεφαλικά κύτταρα και μοιάζει με συνδυασμό άνοιας, Πάρκινσον και νόσου κινητικού νευρώνα.
Μια συναισθηματική ερευνητική ομάδα δάκρυσε καθώς περιέγραφε πώς τα δεδομένα δείχνουν ότι η νόσος επιβραδύνθηκε κατά 75% στους ασθενείς.
Αυτό σημαίνει ότι η πτώση που θα περιμένατε κανονικά σε ένα χρόνο θα διαρκούσε τέσσερα χρόνια μετά τη θεραπεία, προσφέροντας στους ασθενείς δεκαετίες “καλής ποιότητας ζωής”, δήλωσε η καθηγήτρια Σάρα Ταμπρίζι στο BBC News.
Η νέα θεραπεία είναι μια μορφή γονιδιακής θεραπείας που χορηγείται κατά τη διάρκεια 12 έως 18 ωρών λεπτής εγχείρησης στον εγκέφαλο.
Τα πρώτα συμπτώματα της νόσου Χάντινγκτον τείνουν να εμφανίζονται στα 30 ή 40 και είναι κανονικά θανατηφόρα εντός δύο δεκαετιών – ανοίγοντας την πιθανότητα ότι νωρίτερα η θεραπεία θα μπορούσε να αποτρέψει την εμφάνιση συμπτωμάτων.
Η καθηγήτρια Ταμπρίζι, διευθύντρια του Κέντρου Νόσου Χάντινγκτον του Πανεπιστημίου Κολεγίου Λονδίνου, περιέγραψε τα αποτελέσματα ως “θεαματικά”.
“Δεν θα περιμέναμε ποτέ ότι θα βλέπαμε μια επιβράδυνση της κλινικής προόδου κατά 75%,” είπε.
Κανένας από τους ασθενείς που έχουν θεραπευτεί δεν έχει αναγνωριστεί, αλλά ένας αποσύρθηκε ιατρικά και έχει επιστρέψει στη δουλειά. Άλλοι στην κλινική δοκιμή εξακολουθούν να περπατούν, παρά τις προσδοκίες ότι θα χρειάζονταν καροτσάκι.
Η θεραπεία πιθανότατα θα είναι πολύ ακριβή. Ωστόσο, αυτή είναι μια στιγμή πραγματικής ελπίδας σε μια ασθένεια που πλήττει τους ανθρώπους στην καλύτερη ηλικία τους και καταστρέφει οικογένειες.

Η νόσος Χάντινγκτον διατρέχει την οικογένεια του Τζακ Μέι-Ντέιβις. Έχει το ελαττωματικό γονίδιο που προκαλεί την ασθένεια, όπως και ο πατέρας του, Φρεντ, και η γιαγιά του, Τζόις.
Ο Τζακ δήλωσε ότι ήταν “πολύ τρομακτικό και φρικτό” να παρακολουθεί την αμείωτη πτώση του πατέρα του.
Τα πρώτα συμπτώματα εμφανίστηκαν στα τέλη της δεκαετίας του ’30 του Φρεντ, συμπεριλαμβανομένων αλλαγών στη συμπεριφορά και τον τρόπο κίνησης. Τελικά χρειάστηκε 24/7 παρηγορητική φροντίδα πριν πεθάνει στην ηλικία των 54, το 2016.
Ο Τζακ είναι 30, υπάλληλος δικηγόρου, πρόσφατα αρραβωνιασμένος με την Κλόε και έχει συμμετάσχει σε έρευνα στο UCL για να μετατρέψει τη διάγνωσή του σε θετικό.
Αλλά πάντα ήξερε ότι ήταν προορισμένος να μοιραστεί τη μοίρα του πατέρα του, μέχρι σήμερα.
Τώρα λέει ότι η “απόλυτα απίστευτη” ανακάλυψη τον έχει αφήσει “καταβεβλημένο” και ικανό να κοιτάξει στο μέλλον που “φαίνεται λίγο πιο φωτεινό, επιτρέπει να σκέφτομαι ότι η ζωή μου θα μπορούσε να διαρκέσει πολύ περισσότερο”.

Η νόσος Χάντινγκτον προκαλείται από ένα λάθος σε ένα μέρος του DNA μας που ονομάζεται γονίδιο χαντιντίν.
Αν ένας από τους γονείς σας έχει τη νόσο Χάντινγκτον, υπάρχει 50% πιθανότητα να κληρονομήσετε το τροποποιημένο γονίδιο και να αναπτύξετε τελικά και εσείς τη νόσο Χάντινγκτον.
Αυτή η μετάλλαξη μετατρέπει μια κανονική πρωτεΐνη που χρειάζεται στον εγκέφαλο – που ονομάζεται πρωτεΐνη χαντιντίν – σε έναν δολοφόνο νευρώνων.
Ο στόχος της θεραπείας είναι να μειώσει μόνιμα τα επίπεδα αυτής της τοξικής πρωτεΐνης, με μια μόνο δόση.
Η θεραπεία χρησιμοποιεί πρωτοποριακή γενετική ιατρική που συνδυάζει γονιδιακή θεραπεία και τεχνολογίες σιωπηλού γονιδίου.
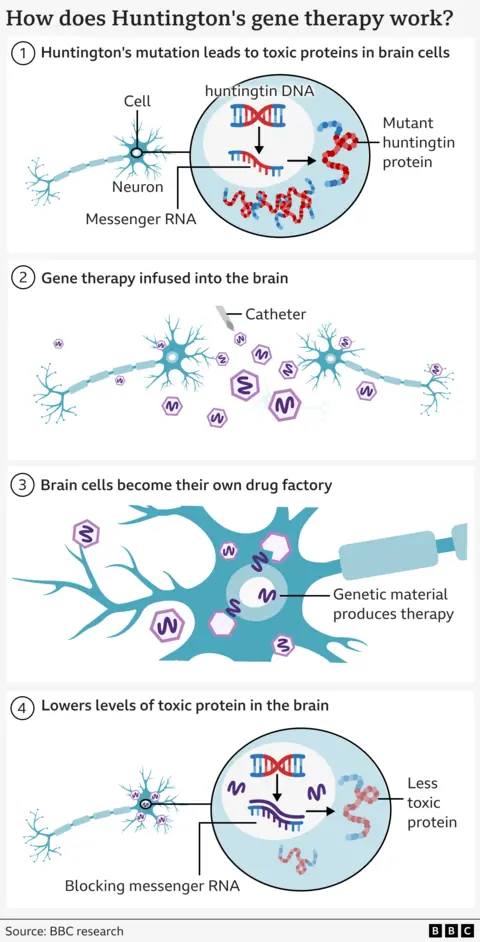
Η θεραπεία ξεκινά με έναν ασφαλή ιό που έχει τροποποιηθεί για να περιέχει μια ειδικά σχεδιασμένη αλληλουχία DNA.
Αυτό εισάγεται βαθιά στον εγκέφαλο χρησιμοποιώντας πραγματικό χρόνο σάρωσης MRI για να καθοδηγήσει έναν μικροκαθετήρα σε δύο περιοχές του εγκεφάλου – τον καυδατικό πυρήνα και τον πυρήνα του θάλαμου. Αυτό απαιτεί 12 έως 18 ώρες νευροχειρουργικής.
Ο ιός στη συνέχεια λειτουργεί σαν μικροσκοπικός ταχυδρόμος – παραδίδοντας το νέο κομμάτι DNA μέσα στα εγκεφαλικά κύτταρα, όπου γίνεται ενεργό.
Αυτό μετατρέπει τους νευρώνες σε εργοστάσιο παραγωγής της θεραπείας για να αποτρέψουν το θάνατό τους.
Τα κύτταρα παράγουν ένα μικρό κομμάτι γενετικού υλικού (που ονομάζεται μικροRNA) που έχει σχεδιαστεί για να παρεμποδίζει και να απενεργοποιεί τις οδηγίες (που ονομάζονται mRNA) που αποστέλλονται από το DNA των κυττάρων για την κατασκευή της μεταλλαγμένης χαντιντίν.
Αυτό έχει ως αποτέλεσμα χαμηλότερα επίπεδα μεταλλαγμένης χαντιντίν στον εγκέφαλο.
Τα αποτελέσματα της δοκιμής – που περιλάμβαναν 29 ασθενείς – έχουν ανακοινωθεί σε δήλωση από την εταιρεία uniQure, αλλά δεν έχουν δημοσιευθεί ακόμα πλήρως για ανασκόπηση από άλλους ειδικούς.
Τα δεδομένα έδειξαν ότι τρία χρόνια μετά τη χειρουργική επέμβαση υπήρξε μέση επιβράδυνση 75% της ασθένειας με βάση μια μέτρηση που συνδυάζει τη γνωστική λειτουργία, τη μηχανική λειτουργία και την ικανότητα διαχείρισης στην καθημερινή ζωή.
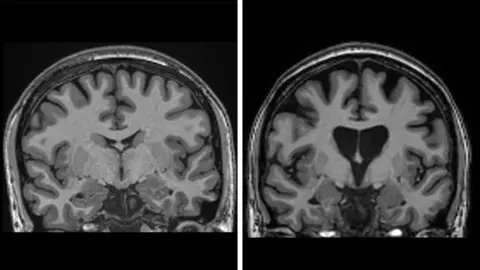
Τα δεδομένα δείχνουν επίσης ότι η θεραπεία σώζει εγκεφαλικά κύτταρα. Τα επίπεδα νευροφιλαμίνων στο εγκεφαλονωτιαίο υγρό – ένα σαφές σημάδι θανάτου εγκεφαλικών κυττάρων – θα έπρεπε να είχαν αυξηθεί κατά το ένα τρίτο αν η ασθένεια συνέχιζε να προχωρά, αλλά ήταν στην πραγματικότητα χαμηλότερα από ό,τι στην αρχή της δοκιμής.
“Αυτό είναι το αποτέλεσμα που περιμέναμε,” δήλωσε ο καθηγητής Έντ Γουάιλντ, σύμβουλος νευρολόγος στο Εθνικό Νοσοκομείο για Νευρολογία και Νευροχειρουργική στο UCLH.
“Υπήρχε κάθε πιθανότητα ότι δεν θα βλέπαμε ποτέ ένα αποτέλεσμα όπως αυτό, οπότε το να ζούμε σε έναν κόσμο όπου ξέρουμε ότι αυτό δεν είναι μόνο δυνατό, αλλά η πραγματική κλίμακα της επίδρασης είναι εκπληκτική, είναι πολύ δύσκολο να το εκφράσουμε πλήρως.”
Είπε ότι ήταν “λίγο δακρυσμένος” σκεπτόμενος την επίδραση που θα μπορούσε να έχει στις οικογένειες.
Η θεραπεία θεωρήθηκε ασφαλής, αν και κάποιοι ασθενείς ανέπτυξαν φλεγμονή από τον ιό που προκάλεσε πονοκεφάλους και σύγχυση που είτε επιλύθηκαν είτε χρειάστηκαν θεραπεία με στεροειδή.
Ο καθηγητής Γουάιλντ αναμένει ότι η θεραπεία “θα διαρκέσει για μια ζωή” καθώς τα εγκεφαλικά κύτταρα δεν αντικαθίστανται από το σώμα με τον ίδιο τρόπο που το αίμα, τα οστά και το δέρμα ανανεώνονται συνεχώς.
Περίπου 75,000 άνθρωποι έχουν τη νόσο Χάντινγκτον στο Ηνωμένο Βασίλειο, τις ΗΠΑ και την Ευρώπη, με εκατοντάδες χιλιάδες να φέρουν τη μετάλλαξη που σημαίνει ότι θα αναπτύξουν τη νόσο.
Η uniQure λέει ότι θα υποβάλει αίτηση για άδεια στις ΗΠΑ το πρώτο τρίμηνο του 2026 με στόχο την κυκλοφορία του φαρμάκου αργότερα εκείνη τη χρονιά. Οι συνομιλίες με τις αρχές στο Ηνωμένο Βασίλειο και την Ευρώπη θα ξεκινήσουν την επόμενη χρονιά, αλλά η αρχική εστίαση είναι στις ΗΠΑ.
Ο Δρ Ουαλί Νάμπι-Σαάμπ, επικεφαλής ιατρικός σύμβουλος της uniQure, δήλωσε ότι ήταν “εξαιρετικά ενθουσιασμένος” για το τι σημαίνουν τα αποτελέσματα για τις οικογένειες, και πρόσθεσε ότι η θεραπεία είχε “τη δυνατότητα να μεταμορφώσει θεμελιωδώς” τη νόσο Χάντινγκτον.
Ωστόσο, το φάρμακο δεν θα είναι διαθέσιμο για όλους λόγω της πολύπλοκης χειρουργικής επέμβασης και του αναμενόμενου κόστους.
“Θα είναι σίγουρα ακριβό,” λέει ο καθηγητής Γουάιλντ.
Δεν υπάρχει επίσημη τιμή για το φάρμακο. Οι γονιδιακές θεραπείες συχνά είναι ακριβές, αλλά η μακροχρόνια επίδρασή τους σημαίνει ότι μπορούν να είναι ακόμα προσιτές. Στο Ηνωμένο Βασίλειο, ο NHS πληρώνει για μια γονιδιακή θεραπεία 2.6 εκατομμυρίων λιρών ανά ασθενή για την αιμορροφιλία B.
Η καθηγήτρια Ταμπρίζι λέει ότι αυτή η γονιδιακή θεραπεία “είναι η αρχή” και θα ανοίξει τις πύλες για θεραπείες που μπορούν να φτάσουν σε περισσότερους ανθρώπους.
Τιμά τους “πραγματικά γενναίους” εθελοντές που συμμετείχαν στη δοκιμή, λέγοντας ότι ήταν “πάρα πολύ χαρούμενη για τους ασθενείς και τις οικογένειες”.
Ήδη εργάζεται με μια ομάδα νέων ανθρώπων που γνωρίζουν ότι έχουν το γονίδιο, αλλά δεν έχουν ακόμα συμπτώματα – γνωστοί ως στάδιο μηδέν Χάντινγκτον – και αποσκοπεί να πραγματοποιήσει την πρώτη δοκιμή πρόληψης για να δει αν η ασθένεια μπορεί να καθυστερήσει σημαντικά ή ακόμη και να σταματήσει εντελώς.
